���̑��̔M�͊w�I��
�M�͊w�̑��@�����
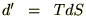 ���
�������g���Ď��̂悤�Ɏ�������܂��B
���
�������g���Ď��̂悤�Ɏ�������܂��B
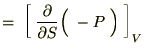
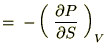
���̂悤�ȊW���������܂��B
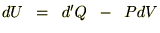
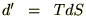 ���
���
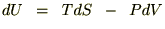

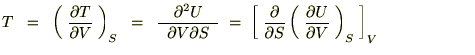
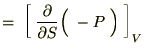
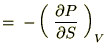
���̂悤�ȊW���������܂��B
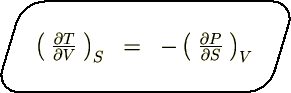
�i�P�j�G���^���s�[�g�̊W��
�܂��G���^���s�[�̎�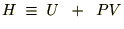 �ɂ��đS�������{���܂��B
�ɂ��đS�������{���܂��B
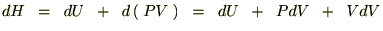
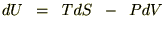 �̎����v���o���A
�̎����v���o���A
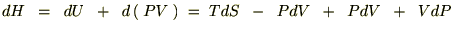
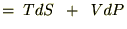
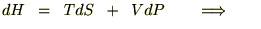 �r�Ƃo���Ɨ��ϐ�
�r�Ƃo���Ɨ��ϐ�
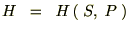 �ƂȂ�A���̂r�Ƃo�ɑ��Ă��ꂼ��Δ������{���܂��B
�ƂȂ�A���̂r�Ƃo�ɑ��Ă��ꂼ��Δ������{���܂��B

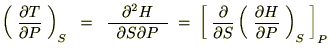
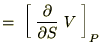
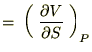
����Ď��̂悤�ȊW����������܂��B
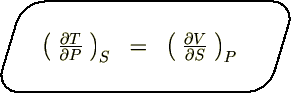
�i�Q�j�w�����z���c�̃t���[�G�i�W�[
�����G�l���M�[�t�ɑ��Ď��̂悤�Ɏ����������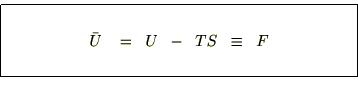
���̂e�ɑ��Ă������悤�ɑS�������{���ƁA
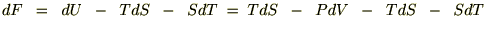
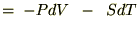
�u�Ƃs���Ɨ��ϐ��ɂȂ�܂��i
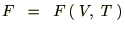 �j�B
�j�B
���ɂ��̂u�Ƃs�Ɋւ��ĕΔ������{���A

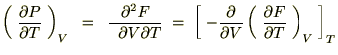
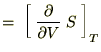
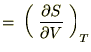
����Ď��̂悤�ȊW����������܂��B
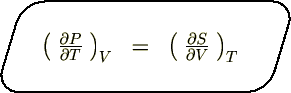
�i�R�j�M�u�X�̃t���[�G�i�W�[
�w�����z���c�̃t���[�G�i�W�[�Ɏ��̂悤�Ɏ�����������A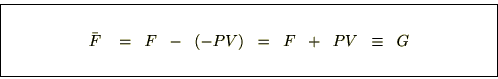
�����悤�ɂ��̂f�ɂ��S�������{���܂��B
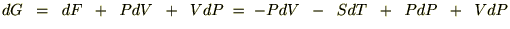
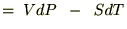
���̂悤�ɂȂ�̂łf�͓Ɨ��ϐ����o�Ƃs�̊��Ƃ��ĕ\���ł��邱�ƂɂȂ�܂��i
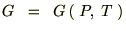 �j�B
�j�B���́g�f�h�ɑ��Ăs�Ƃo�Ɋւ��ĕΔ������{���A

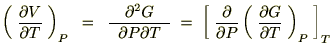
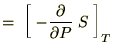
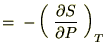
����Ď��̂悤�ȊW���������܂��B
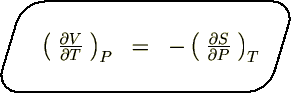
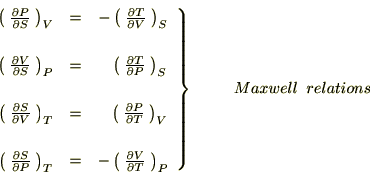
���̑��̍l�@
�N���E�W�E�X�̕s�����́A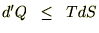
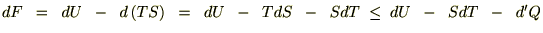
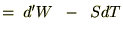
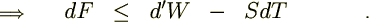
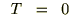 �ł���̂ŁA
�ł���̂ŁA
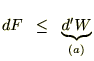
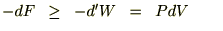 �E�E�E�E�E�E�@�@�@�@�O�Ɍ������čs���d��
�E�E�E�E�E�E�@�@�@�@�O�Ɍ������čs���d��
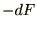 �͂e�̌����ʂ��Ӗ����Ă��܂��B
�͂e�̌����ʂ��Ӗ����Ă��܂��B
����ɃM�u�X�̃t���[�G�i�W�[�Ɋւ��ẮA�w�����z���c�̃t���[�G�i�W�[��
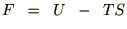 �ł���̂ł����������ƁA
�ł���̂ł����������ƁA
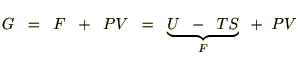
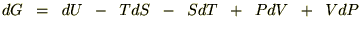
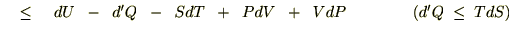
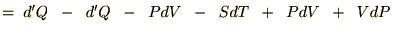
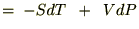
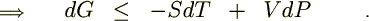
�艷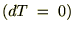 �ł��舳
�ł��舳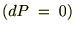 �̌��ł̕ω��ł́A
����ɂ��A
�ł���Ƃ����܂��B
�̌��ł̕ω��ł́A
����ɂ��A
�ł���Ƃ����܂��B
���Ȃ݂ɒP�ʎ��ʂ�����̂f���ʂŕ\�������́A
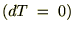 �ł��舳
�ł��舳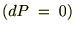 �̌��ł̕ω��ł́A
�̌��ł̕ω��ł́A
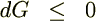
���f�͕K������
�Ƃ������Ƃ������܂��B�ω����~�܂��ĕ��t��ԂɂȂ�� �f�̒l���ɏ��l
�f�̒l���ɏ��l
���Ȃ݂ɒP�ʎ��ʂ�����̂f���ʂŕ\�������́A
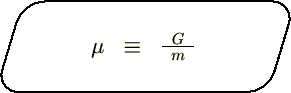
�}�b�N�X�E�F���W���̊ȒP�Ȋo����
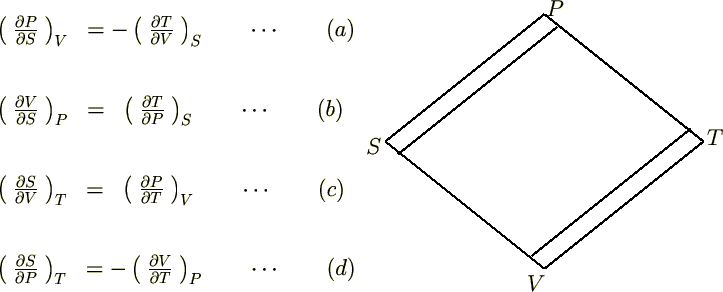
(a)�̎�����������Ă����ƁA�܂��o����r�ւ������Ԃ��l���A�����q������Ƃ�������ɂ��ĕΔ��������肳��ɂr�̈ʒu����E���ֈړ�����Ƃu�ɓ˂�������܂��������
 �ɂ�����Y�����̂u�ɑΉ������܂��B
�ɂ�����Y�����̂u�ɑΉ������܂��B
���x�͂��̔��Α��̕ӂɂ����Đ�قǂƓ����o����r�ֈړ������悤�ɓ��������ɂs����u�ֈړ�����Δ���
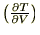 �����܂��B�����悤�ɂs���u���r�Ƃ����������ōl����̂œY�����̋L���͂r�ɂȂ�܂��B
�����܂��B�����悤�ɂs���u���r�Ƃ����������ōl����̂œY�����̋L���͂r�ɂȂ�܂��B
����ɕ����Ɋւ��Ă͂o�|�r�Ƃs�|�u�̕ӂ�����Ɠ����ɂ�����{�̐��������Ă��܂����A������}�C�i�X�\���̂��߂́g���邵�h�ƍl���Ă��������B���̂悤�Ȃ����ŏo���オ��̂�(a)�̎��A
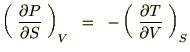
���x��(b)�̎��ɂ��Ă���Ă݂�ƁA�܂��u���r���
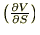 �ƂȂ肳��ɐ}���u���r���g�o�h�ƂȂ��Ă���̂ł��̕Δ����ɂ�����Y�����͂o��Ή������܂��B�����Ău���r�̕ӂ̔��Α��̕ӂ����Ă݂�ƁA�s���o�ƂȂ��Ă���̂ł��̂s�Ƃo�̕Δ���������A�����Ăs���o���g�r�h�ƂȂ��Ă���̂ł��̏ꍇ�̓Y�����͂r�ɂȂ�܂��B�܂��A�u���r�A�s���o�̕ӂ̓����ɂ͂�����{�̐����Ȃ��̂ł���́g�v���X�h�̎��Ȃƍl���Ă��������B����Ď��̂悤�ɋ��܂�܂��B
�ƂȂ肳��ɐ}���u���r���g�o�h�ƂȂ��Ă���̂ł��̕Δ����ɂ�����Y�����͂o��Ή������܂��B�����Ău���r�̕ӂ̔��Α��̕ӂ����Ă݂�ƁA�s���o�ƂȂ��Ă���̂ł��̂s�Ƃo�̕Δ���������A�����Ăs���o���g�r�h�ƂȂ��Ă���̂ł��̏ꍇ�̓Y�����͂r�ɂȂ�܂��B�܂��A�u���r�A�s���o�̕ӂ̓����ɂ͂�����{�̐����Ȃ��̂ł���́g�v���X�h�̎��Ȃƍl���Ă��������B����Ď��̂悤�ɋ��܂�܂��B
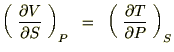
���̂悤�ɂ���A�E��̂Ђ��`�̐}�`������������o���Ă����@�B�I�Ƀ}�b�N�X�E�F���̊W�������߂���Ƃ������Ƃ��킩�邩�Ǝv���܂��B

�}�b�N�X�E�F���̊W���֘A�y�[�W
- ��ԕ�����
- ���낢��Ȕ������������������T�C�g�ł��B�l�I�Ȏ�̗̈�ł���Ă���̂ł��Ȃ�E���������e�����邩�Ǝv���܂����A���̂ւ�̂Ƃ���͐�������������C�ł��Ȃ������܂��B
- �}�b�N�X�E�F���̑��x���z��
- ���낢��Ȕ������������������T�C�g�ł��B�l�I�Ȏ�̗̈�ł���Ă���̂ł��Ȃ�E���������e�����邩�Ǝv���܂����A���̂ւ�̂Ƃ���͐�������������C�ł��Ȃ������܂��B
- �ő̌��q�̔M�U��
- ���낢��Ȕ������������������T�C�g�ł��B�l�I�Ȏ�̗̈�ł���Ă���̂ł��Ȃ�E���������e�����邩�Ǝv���܂����A���̂ւ�̂Ƃ���͐�������������C�ł��Ȃ������܂��B











